При травме мозга белок свертывания крови приводит к потере нейронов
Черепно-мозговая травма может иметь серьезные последствия для когнитивных функций, в том числе стать причиной развития нейродегенеративных процессов. Авторы статьи в Journal of Neuroinflammation считают, что повреждение нейронов вызывается белком свертывания крови фибрином, который попадает в ткани мозга при травме и запускает воспалительный и иммунный ответы организма.
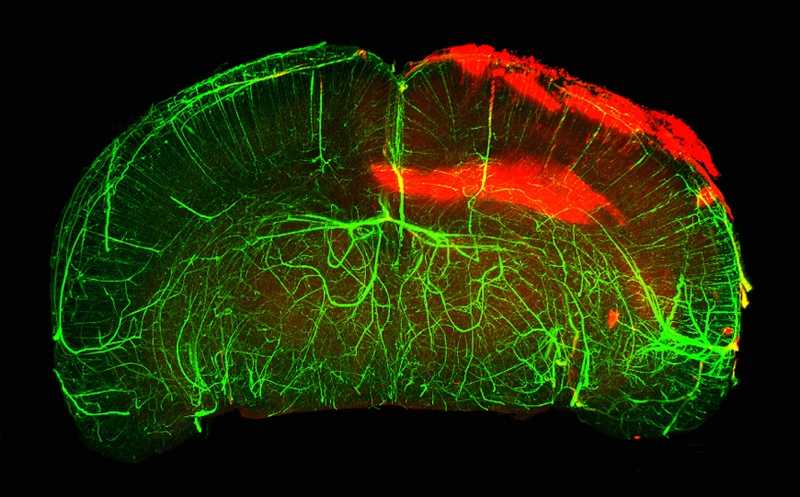
При травматическом повреждении сосудов из растворимого фактора свертывания крови фибриногена образуется нерастворимый белок фибрин, который сразу после травмы формирует тромбы и закупоривает сосуды, останавливая кровотечение. Ученые из Калифорнийского университета в Сан-Диего обнаружили, что фибрин, образующийся при черепно-мозговой травме (ЧМТ), откладывается в тканях мозга и запускает процессы врожденного иммунитета, аналогичные тем, что наблюдаются при неврологических заболеваниях — инсульте, рассеянном склерозе и т.д. Вызванное фибрином нейровоспаление может иметь серьезные последствия для неврологических функций, в том числе повышать риск развития болезни Альцгеймера.
Иммуногистохимические исследования проводились на образцах тканей головного мозга самцов мышей линии C57BL/6. Также из NIH NeuroBioBank были получены образцы мозга людей с ЧМТ: один образец («острая ЧМТ») был взят у 32-летнего мужчины с огнестрельным ранением головы, другой («хроническая ЧМТ») — у 21-летней женщины, прожившей год после травмы головы, нанесенной тупым предметом. В ткани мозга мышей вводили меченый фибриноген, а через два дня после ЧМТ делали слепки сосудов головного мозга. Кроме того, из пораженных участков отбирали образцы разных видов клеток (миелоидные клетки, микроглия и др.) для РНК-секвенирования.
Эксперименты с окрашиванием фибриногена (фибрина) показали, что при ЧМТ происходит его экстравазация в ткани мозга человека, где наблюдается рекрутирование и активация иммунных клеток, экспрессирующих Iba1 и MRP14 — маркеры активации микроглии и инфильтрации моноцитов, как при болезни Альцгеймера и рассеянном склерозе.
Фибрин активирует систему врожденного иммунитета центральной нервной системы через экспрессируемый микроглией и моноцитами рецептор интегрина CD11b/CD18. Взаимодействие гамма-цепи фибрина с CD11b приводит к активации провоспалительных и прооксиндантных генов, связанных с воспалением, каскадом MAPK и регуляцией метаболизма активных форм кислорода (АФК). То есть отложение фибрина при ЧМТ способствует развитию нейротоксичных процессов, приводящих к повреждению коры головного мозга.
Нарушение гематоэнцефалического барьера, экстравазация фибрина и последующая активация врожденного иммунного ответа, по мнению ученых, является общим механизмом для разных неврологических заболеваний. Данный механизм может стать терапевтической мишенью при ЧМТ. Конечно, нужно предварительно определить оптимальное терапевтическое окно: избирательное воздействие на фибрин дает возможность подавить активность нейродегенеративных генов без полной инактивации систем врожденного иммунитета, однако повышает риск развития внутричерепного кровоизлияния.
Таким образом, исследования показали, что ЧМТ может вызывать как острое, так и хроническое повреждение гематоэнцефалического барьера с отложением фибрина в тканях мозга и активацией врожденного иммунитета в тканях центральной нервной системы. Как результат, развивается нейротоксическое поражение тканей мозга, которое в будущем грозит развитием нейродегенеративных заболеваний, в том числе деменции.
Просачивание белков крови в мозг индуцирует нейротоксическую активность микроглии
Dean T., et al. Fibrin promotes oxidative stress and neuronal loss in traumatic brain injury via innate immune activation // Journal of Neuroinflammation. 2024. 21, 94. DOI: 10.1186/s12974-024-03092-w








 Меню
Меню





 Все темы
Все темы





 0
0