Генноотредактированные В-клетки — фабрики лекарственных белков в организме
Характеристики иммунного ответа на вакцину против патогена значительно варьируют. Авторы статьи в Science предложили, как сделать его предсказуемым. Они получили мышей с отредактированными В-клетками, которые экспрессировали широконейтрализующие антитела против белков патогенов. Наличие таких клеток в организме обеспечило эффективность вакцинации — в ответ на антиген эти клетки активировались и размножались, а уровень нейтрализующих антител поднимался до терапевтического. Концепцию проверили на антителах против ВИЧ-1, вирусов гриппа и малярийного плазмодия.
Исследователи из Рокфеллеровского университета (Нью-Йорк) и других научных центров предложили оригинальный подход к защите от инфекций — введение в организм отредактированных клеток-предшественников В-лимфоцитов, вырабатывающих эффективные защитные антитела, в сочетании с вакцинацией. Присутствие в крови таких клеток гарантирует появление широконейтрализующих антител, а их терапевтические концентрации достигаются естественным путем, когда антиген вызывает активацию и размножение В-клеток.
В работе участвовал Флориан Краммер из Школы медицины Айкана в Маунт-Синай, специалист по респираторным вирусным инфекциям, чьи аналитические комментарии по разработке вакцин против коронавируса SARS-CoV-2 получили широкую известность во время пандемии. (Сейчас он работает в Австрии, в Венском медицинском университете.)
После инфекции или вакцинации в крови человека появляются антитела к патогену. Однако против многих инфекционных агентов, включая ВИЧ-1, вирус гриппа или малярийного плазмодия, не удается получить длительную и эффективную защиту. Тем не менее у некоторых людей вырабатываются так называемые широконейтрализующие антитела (ШНАТ), активные против различных линий патогена и способные лечить инфекцию при пассивном введении другим. Выработка ШНАТ — одна из важных целей разработчиков вакцин, но ее трудно достичь. Например, эпитопы ВИЧ, против которых могли бы вырабатываться ШНАТ, бывают замаскированы гликозилированием.
Альтернативным подходом могут стать генноотредактированные B-клетки, производящие в организме терапевтические антитела (или другие белки). Все клетки крови, включая В-лимфоциты, развиваются из гемопоэтических стволовых клеток. После вакцинации субпопуляция В-клеток, специфичных к вакцинному антигену, размножается. При этом формируется популяция плазматических клеток, которые способны секретировать до 10000 молекул антитела в секунду и выживать в костном мозге годами, что обеспечивает длительную защиту. Этот механизм можно использовать для производства терапевтических белков прямо в организме. Таких преимуществ, как у плазматических клеток, нет у других распространенных мишеней генного редактирования, например, у гепатоцитов или миоцитов, подчеркивают авторы статьи в Science.
Иммуноглобулиновый локус гемопоэтических стволовых и прогениторных клеток (ГСПК) мышей авторы редактировали с помощью CRISPR-Cas9. Таким способом они получили клетки, продуцирующие анти-ВИЧ-1-антитело 3BNC117. Отредактированные ГСПК вводили мышам, и уже in vivo они превращались в B-клетки. Затем мышей иммунизировали антигеном ВИЧ-1, эти В-клетки активировались, подвергались клональному размножению и развивались в специфические плазматические клетки.
Таким способом авторам удалось получить высокие уровни сывороточных антител против ВИЧ-1, малярии и вируса гриппа. Очень небольшого количества отредактированных ГСК (около 7000) было достаточно для достижения терапевтических концентраций антител. Полученные титры были достаточно высокими для нейтрализации ВИЧ-1, ингибирования проникновения малярийного плазмодия в гепатоциты и защиты мышей от летальной инфекции вирусами гриппа.
Один из многообещающих подходов к созданию эффективной вакцины против ВИЧ связан с продукцией ШНАТ, к которой ведет соматическая гипермутация — накопление мутаций в генах иммуноглобулинов В-клеток, способствующих созреванию аффинности. Однако «подавляющее большинство соматических гипермутаций вредно, незаметно или неэффективно», отмечают авторы. Присутствие в организме В-клеток, которые уже способны экспрессировать ШНАТ к ВИЧ-1 (возможно, нескольких типов таких клеток), может быть лучшей альтернативой.
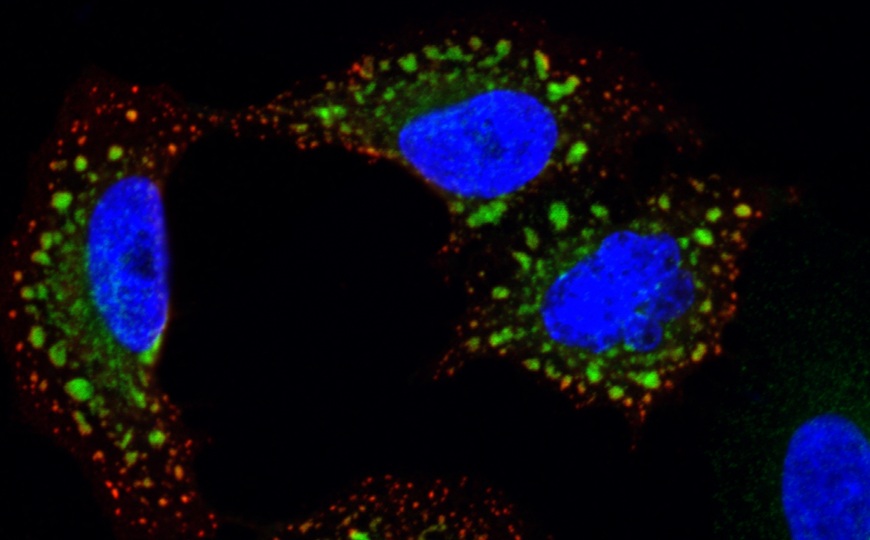
Чтобы наблюдать за развитием отредактированных клеток, в одном из экспериментов авторы ввели в ГСПК ген химерного белка — антитела с флуоресцентным белком. Экспрессия такого белка была высокой, что указывает на дополнительные возможности, например, создание В-клеток, которые производили бы антитела, несущие терапевтический белок.
Аналогичным образом авторы отредактировали человеческие ГСК, которые развились в человеческие В-лимфоциты, экспрессирующие специфические антитела, в организме иммунодефицитных мышей. Они также показали, что можно ввести в организм сразу два клона отредактированных ГСПК, которые производят разные антитела к одному белку патогена.
Таким образом, предложена парадигма клеточной терапии для профилактики или лечения заболеваний с использованием «самовоспроизводящихся белковых фабрик» — модифицированных В-клеток. По мнению авторов, этот подход идеален также для прямого редактирования in vivo. Даже если будет отредактировано очень малое количество клеток, последующая амплификация под воздействием антигена многократно увеличит их популяцию.
Эпитоп ВИЧ, лишенный ключевого гликана, может стать основой для вакцины
Источник
Harald Hartweger, et al. B lymphocyte protein factories produced by hematopoietic stem cell gene editing // Science. 16 Apr 2026. Vol 392, Issue 6795. DOI: 10.1126/science.adz89


 Меню
Меню





 Все темы
Все темы




 0
0