Новые препараты против ВИЧ заставили зараженные клетки предъявлять вирусные антигены Т-лимфоцитам
Сотрудники Питтсбургского университета и компании Fox Chase Therapeutics Discovery создали кандидатные препараты, которые делают клетки, зараженные ВИЧ, видимыми для иммунной системы. Эти препараты стимулируют уничтожение в клетке белка, подавляющего экспрессию вирусных антигенов на поверхности клетки. Такой подход может открыть путь к устранению резервуаров ВИЧ в организме, недоступных для существующих антивирусных препаратов.
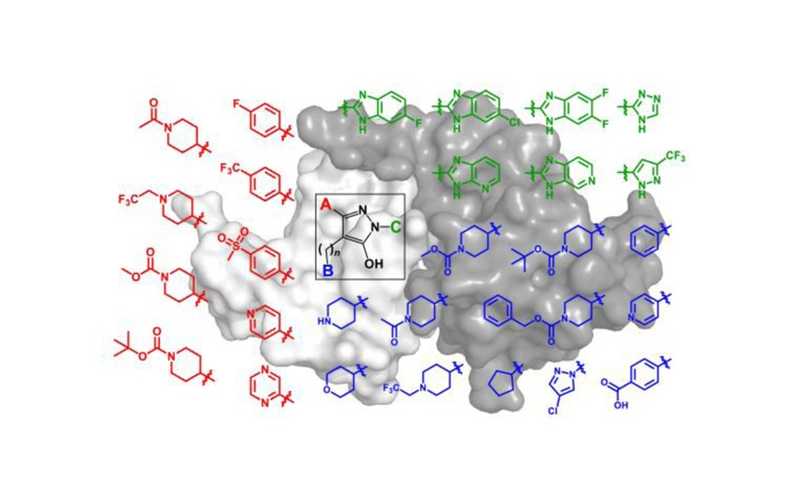
Самой сложной задачей был поиск вещества, избирательно связывающееся с Nef
Credit:
ACS Infect Dis. 2020. DOI: 10.1021/acsinfecdis.9b00382
Команда руководителя работы Томаса Смитгалла из Медицинской школы Питтсбургского университета много лет изучает Nef — белок ВИЧ, экспрессирующийся на высоких уровнях после начала инфекции. Гены nef лентивирусов приматов ВИЧ-1, ВИЧ-2 и SIV кодируют мембраносвязанные белки, играющие ключевую роль в репликации, персистенции и распространении вируса. Nef-дефектный ВИЧ-1 плохо реплицируется в организме гуманизированных мышей и не вызывает потери CD4+ Т-клеток, в отличие от вируса дикого типа. Известно, что Nef подавляет экспрессию на поверхности клетки молекул главного комплекса гистосовместимости MHC-I, которые должны презентировать вирусные антигены цитотоксическим Т-лимфоцитам, атакующим зараженные клетки.
Таким образом, Nef предотвращает атаку иммунной системы на резервуар ВИЧ, и не удается достичь полного излечения. Даже если вирус не определяется в крови пациента, прекращение антиретровирусной терапии приведет к новому всплеску его репликации.
Ранее авторы установили, что соединения на основе гидроксипиразола связываются с Nef, ингибируют Nef-зависимое усиление инфекционности ВИЧ-1, репликацию и частично обращают вспять опосредованное Nef подавление экспрессии MHC-I. Однако Nef — неподходящая мишень для ингибирования малыми молекулами, потому что у него нет активного центра, в отличие, например, от ферментов. Существующие ингибиторы, даже те, которые селективно распознают именно этот белок, блокируют одни его функции, но не затрагивают другие.
В этот раз исследователи избрали другой подход: они направили Nef на деградацию в протеасоме с помощью убиквитиновой метки. При участии сотрудников компании Fox Chase Therapeutics Discovery (FCTDI) они сконструировали вещества, способные выполнять эту задачу. Молекулу на основе гидроксипиразола связали гибкими полиэтиленгликолевыми линкерами с лигандами для комплекса, включающего в себя убиквитинлигазу Е3. Такая конструкция прикрепляет убиквитинлигазу к Nef, в результате происходит прикрепление убиквитинов к Nef, которое ведет к его деградации. Авторы синтезировали более ста подобных молекул и отобрали среди них наилучшие. Интересно, что среди лигандов для убиквитинлигазного комплекса были производные талидомида — вещество с ужасной репутацией не впервые используется в разработке лекарственных препаратов, и при должном проведении клинических испытаний это нормально.
Подобные препараты относятся к категории «химер, нацеленными на протеолиз» (proteolysis targeting chimeras, PROTAC). PCR.NEWS ранее писал о живой вакцине против гриппа на основе вируса с PROTAC-компонентом, направляющим вирусные белки на протеолиз.
Молекулы PROTAC вызвали деградацию Nef и восстановили сниженную экспрессию рецепторов MHC-I и CD4 в Т-клетках. Более того, они подавляли репликацию ВИЧ-1 в донорских мононуклеарных клетках периферической крови. Таким образом, есть основания считать, что таргетная деградация Nef поможет отменить латентное состояние ВИЧ, восстановить адаптивные иммунные реакции против зараженных клеток in vivo и устранить резервуары в организме.
«Найти малую молекулу, которая избирательно связывается с Nef, было самой сложной задачей, — говорит Томас Смитгалл. — Теперь нам нужно продолжить оптимизацию медицинской химии и посмотреть, насколько хорошо она работает против резервуара ВИЧ на животной модели».
В ходе доклинических испытаний на животных исследователи планируют картируовать сигнальные пути Nef, чтобы точно узнать, как PROTAC работают в клетках, и определить структуру белка Nef в комплексе с молекулой PROTAC и клеточным механизмом, ответственным за его деградацию.
Источники
Lori A. Emert-Sedlak, et al. PROTAC-mediated degradation of HIV-1 Nef efficiently restores cell-surface CD4 and MHC-I expression and blocks HIV-1 replication // Cell Chemical Biology. 2024. DOI: 10.1016/j.chembiol.2024.02.004
Статья на bioRxiv
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0