Терапевтические вакцины против ВПЧ-ассоциированного рака: структура имеет значение
Несколько профилактических вакцин против онкогенных подтипов вируса папилломы человека (ВПЧ) разрешены к применению. Однако одобренных терапевтических вакцин, которые вызывали бы уничтожение ВПЧ-ассоциированных опухолей, пока не существует, хотя разработки ведутся. Ученые из Северо-Западного университета (США) показали, что эффективность такой вакцины можно повысить, изменяя не состав, а структуру иммуногенных наночастиц. Вариант вакцины, в котором антигенный пептид ВПЧ был прикреплен к адъювантной ДНК через N-конец, оказался более иммуногенным, чем все другие варианты, в экспериментах на клетках, опухолевых сфероидах и мышиных моделях.
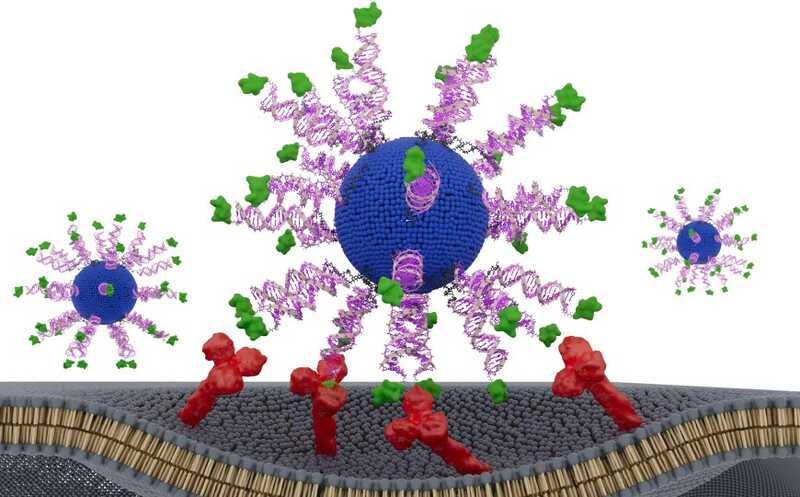
Сферическая наночастица нуклеиновых кислот (SNA), несущая антиген ВПЧ и адъювантную ДНК, взаимодействует с рецептором клетки, что приводит к ее поглощению и противоопухолевому антиген-специфическому ответу CD8⁺ Т-клеток.
Credit:
Connor Forsyth, Jake Cohen | Mirkin Research Group/Northwestern University | Пресс-релиз
Исследователи из Северо-Западного университета (США) сконструировали вакцину, которая усиливает иммунный ответ против опухолей, вызванных вирусом папилломы человека (ВПЧ). Это часть их многолетней работы с иммуногенными сферическими наночастицами нуклеиновых кислот (SNA). В новом исследовании они доказали, что эффективность вакцины в значительной мере зависит от ориентации опухолевого пептидного антигена, который несут наночастицы.
SNA изобрел Чад Миркин из Северо-Западного университета, руководитель данной работы и пионер структурной наномедицины — направления, которое исследует влияние конфигураций биомолекул и их комплексов на свойства лекарственного препарата. Вакцины в том числе противораковые, обычно содержат смесь компонентов, например, антигенов и адъюванта. Даже самые современные препараты не используют или мало используют возможности структурирования, и «для создания наиболее эффективных вакцин против рака нам придется это сделать», говорит Миркин.
Команда под руководством Чада Миркина уже разработала SNA-вакцины против нескольких видов рака, включая меланому, трижды негативный рак молочной железы, рак толстой кишки, рак предстательной железы и карциному Меркеля. Все они показали многообещающие результаты в доклинических моделях, и некоторые проходят клинические исследования.
Теперь исследователи ищут подходы к вакцине против ВПЧ-ассоциированных опухолей. Онкогенные подтипы ВПЧ не только вызывает большинство случаев рака шейки матки, но и раки головы и шеи; только в США ежегодно регистрируется около 18 000 новых случаев рака этого типа. Существующие профилактические вакцины против ВПЧ, такие как Гардасил или российская вакцина Цегардекс, могут предотвратить вирусную инфекцию, однако терапевтических вакцин, вызывающих иммунный ответ против уже существующей опухоли, пока нет. Подавляющее большинство пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи в итоге умирает от него.
Терапевтические противоопухолевые вакцины обучают цитотоксические CD8+ Т-клетки распознавать и уничтожать раковые клетки. Клетки ВПЧ-позитивных опухолей головы и шеи экспрессируют вирусные онкобелки E6 и E7. Перспективную мишень для иммунотерапии представляет собой эпитоп E711-19 (участок белка E7, содержащей аминокислотные остатки с 11-го по 19-й), который и выбрали авторы исследования.
Каждая наночастица содержит липосомное ядро, покрытое «шубой» из иммуноактивирующих молекул ДНК (CpG-ДНК), и короткий фрагмент белка ВПЧ. Эти SNA поглощаются антигенпрезентирующими клетками, такими как дендритные клетки, что усиливает активацию противоопухолевых Т-клеток.
Все три варианты вакцины содержали одни и те же ингредиенты. Единственное различие заключалось в расположении и ориентации антигенного пептида. В одном варианте он находился внутри наночастицы, в двух других — на поверхности, причем был прикреплен к ДНК или N-концом, или C-концом. Каждый из вариантов протестировали на клетках in vitro, а также на гуманизированных мышиных моделях ВПЧ-ассоциированного рака, и на сфероидах, полученных из клеток человеческих опухолей головы и шеи.
Все варианты усиливали активацию дендритных клеток и цитотоксичность CD8+ Т-клеток человека по сравнению со смесью пептида и CpG-ДНК. Однако вариант с прикреплением пептида через N-конец существенно превосходил другие по иммуногенности. Например, цитотоксические Т-клетки, активированные этим вариантом, вырабатывали примерно в восемь раз больше ключевого противоопухолевого цитокина интерферона-гамма по сравнению с двумя другими вариантами, и гораздо успешнее уничтожали раковые клетки.
У мышей этот вариант также оказался наиболее действенным: рост ВПЧ-ассоциированных опухолей значительно замедлился, выживаемость увеличилась. (Медианная выживаемость составила 33 дня в группе, получившей вакцину с прикреплением антигена через N-конец, 30 дней — у получивших два других варианта, и 28 — у получивших смесь антигена с адъювантом или «пустой» буферный раствор). Он также вызвал наиболее выраженные изменения транскрипции в CD8 + Т-клетках мышей. В опухолевых сфероидах, полученных от трех пациентов с ВПЧ-ассоциированным раком, этот вариант вакцины уничтожил в 2,5 раза больше раковых клеток.
«Этот эффект не был достигнут за счет добавления новых ингредиентов или увеличения дозы, — подчеркнул соруководитель работы Йохен Лорч. — Он возник благодаря более продуманной презентации тех же компонентов. Иммунная система чувствительна к геометрии молекул».
Хотя общая величина активации иммунной системы in vivo всех исследуемых конструкций была умеренной, определенная ориентация антигена улучшила сразу несколько показателей эффективности, подчеркивают авторы. Возможно, доступность С-конца имеет решающее значение для расщепления в протеасоме и последующего связывания фрагментов с MHC-I.
Авторы планируют с помощью структурного подхода усовершенствовать вакцины, которые представлялись многообещающими, но не смогли вызвать достаточно сильный иммунный ответ у пациентов. Чад Миркин считает, что в поиске наиболее эффективных вариантов решающую роль могут сыграть ИИ-алгоритмы.
Попытки разработать терапевтические вакцины против ВПЧ, в том числе на платформе мРНК, предпринимались неоднократно. В 2019 году PCR.news писал о терапевтической вакцине типапкиноген совацивек (TG4001) против ВПЧ-ассоциированных опухолей на основе вирусного вектора MVA, которая показала хорошие результаты при цервикальных дисплазиях. К сожалению, она не увеличила выживаемость без прогрессирования у пациентов с рецидивирующим или метастатическим раком шейки матки и аногенитальной области по сравнению с монотерапией авелумабом. Разработчик, французская компания Transgene, в настоящее время сосредоточила усилия на других препаратах, включая TG4050, персонализированную вакцину для лечения рака головы и шеи.
Источники
Jeongmin Hwang, et al. E711-19 placement and orientation dictate CD8+ T cell response in structurally defined spherical nucleic acid vaccines // Science Advances. 11 Feb 2026. Vol 12, Issue 7. DOI: 10.1126/sciadv.aec3876
Цитаты по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0