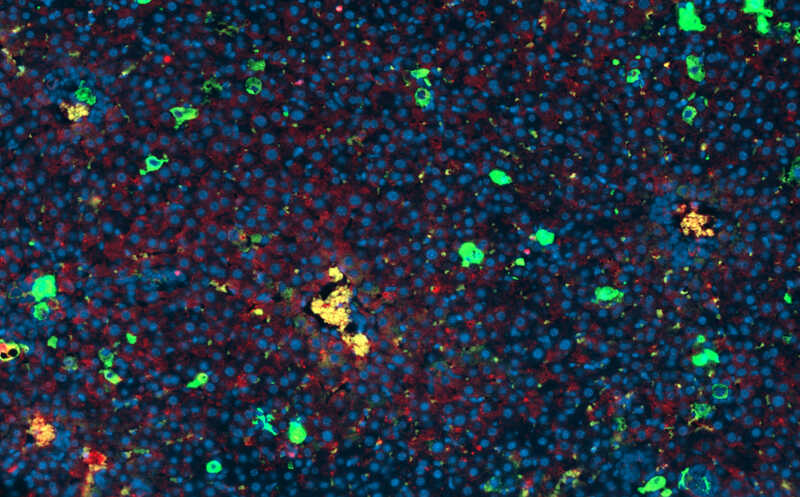
Т-клетки при хроническом лимфолейкозе теряют функциональность из-за недостатка холестерина
Ученые из Нидерландов обнаружили, что T-клетки при хроническом лимфолейкозе страдают от нехватки липопротеинов низкой плотности (LDL), из-за чего их способность к активации и пролиферации снижается. Как следствие, нарушение липидного обмена Т-клеток ослабляет противоопухолевый иммунный ответ. Авторы статьи предполагают, что повышение доступности LDL для Т-клеток или активация в них окисления жирных кислот усилят иммунотерапию, однако для подтверждения этого требуются дальнейшие исследования.
Хронический лимфолейкоз (ХЛЛ) — наиболее распространенный лейкоз у людей европейского происхождения, характеризующийся накоплением злокачественных В-клеток. Современные средства терапии, такие как ингибиторы тирозинкиназы Брутона (BTK) или Bcl-2, значительно улучшают прогноз, но не приводят к полному излечению пациентов. Одна из причин состоит в дисфункции Т-лимфоцитов, которая вызвана их взаимодействием со злокачественными клетками. Недавние исследования показали, что липидный обмен играет важную роль в активации и функции Т-клеток, однако его влияние при ХЛЛ изучено недостаточно.
Чтобы подробнее охарактеризовать вклад липидного обмена в работу Т-клеток при ХЛЛ, ученые из Нидерландов сравнили пролиферацию и активацию Т-лимфоцитов здоровых доноров и доноров с ХЛЛ на обычной и обедненной липопротеинами низкой плотности (LDL) среде. На обычной среде клетки пациентов с ХЛЛ росли медленнее и активируются слабее по сравнению с клетками здоровых доноров. При дефиците LDL обе линии клеток полностью останавливали пролиферацию и снижали уровень активации по сравнению с клетками на обычной среде. Однако когда в обедненную среду дополнительно вносили LDL, пролиферация и активация клеток восстанавливалась до контрольных уровней.
Убедившись в важности экзогенного холестерина для активации Т-клеток, авторы проверили, с чем связано меньшее усвоение холестерина лимфоцитами при ХЛЛ и, как следствие, меньшая их активация. При помощи проточной цитометрии они оценивали концентрацию рецепторов липопротеинов (LDLR) на мембране клеток. На Т-клетках здоровых доноров число рецепторов стабильно возрастало при активации, а у лимфоцитов пациентов с ХЛЛ этот ответ был серьезно снижен.
Транскриптомный анализ показал, что в покоящихся Т-лимфоцитах пациентов с ХЛЛ изменена экспрессия 119 генов-участников ключевых метаболических путей липидов. Уровень экспрессии транспортеров холестерина ABCA1 и ABCG1 и синтазы жирных кислот FASN был снижен, а скваленэпоксидазы SQLE — фермента, ограничивающего скорость биосинтеза холестерина, — повышен. В активированных лимфоцитах выявили 74 дифференциально экспрессирующихся гена. При ХЛЛ также снижалась экспрессия транспортеров холестерина и жирных кислот, некоторых факторов транскрипции групп SREBP (белки, связывающие регуляторный элемент стерола) и PPAR (рецепторы, активируемые пероксисомными пролифераторами). По полученным результатам ученые сделали вывод о нарушениях синтеза жирных кислот и холестерина, а также ограниченном катаболизме липидов.
Далее исследователи предположили, что если в лимфоцитах пациентов с лимфолейкозом нарушен синтез определенных липидов, то их внутриклеточное содержание должно быть снижено по сравнению со «здоровыми» Т-лимфоцитами. При помощи флуоресцентного окрашивания и конфокальной микроскопии они установили, что, вопреки ожиданиям, и покоящиеся, и активированные клетки при ХЛЛ накапливают в себе больше жировых капель, чем контрольные. Такие жировые капли в основном характерны для адипоцитов. Масс-спектрометрический анализ липидного состава показал, что в Т-клетках при ХЛЛ на фоне стимуляции уменьшается содержание фосфатидилхолина и сфингомиелина. В то же время нейтральные липиды, особенно триглицериды, активнее накапливаются в этих клетках. Было выявлено снижение экспрессии фермента ATGL, отвечающего за липолиз, что может ограничивать расщепление триглицеридов. Ингибирование ATGL в здоровых Т-клетках привело к накоплению липидов, подтверждая роль этого фермента в регуляции липолиза. Также в Т-клетках пациентов с ХЛЛ снижалась активность β-окисления жирных кислот, что сопровождалось накоплением ацилкарнитинов. Эти нарушения могут объяснять снижение активации и пролиферации Т-клеток у пациентов с лимфолейкозом.
Дальнейшие эксперименты показали, что нарушение окисления жирных кислот ослабляет активацию Т-клеток, но не влияет на их пролиферацию. Однако уменьшение уровня холестерина препятствовало формированию липидных рафтов — микрообластей мембраны, необходимых для сигналинга при активации Т-клеток. Конфокальная микроскопия выявила уменьшение их количества и ослабление кластеризации при ХЛЛ. Предварительное изъятие холестерина из мембран подавляло пролиферацию Т-клеток при ХЛЛ, но не влияло на здоровые Т-клетки.
Таким образом, нарушения липидного обмена в Т-клетках при ХЛЛ делают их более уязвимыми к снижению уровня холестерина и усугубляют функциональную недостаточность. Понимание этих клеточных механизмов открывает перспективы для разработки методов лечения, связанных с коррекцией уровня доступного для Т-клеток холестерина или активацией окисления жирных кислот.
Клетки острого миелоидного лейкоза изолируют мРНК онкосупрессоров, чтобы выжить
Источник
Chaja Jacobs, et al. Cholesterol homeostasis and lipid raft dynamics at the basis of tumor-induced immune dysfunction in chronic lymphocytic leukemia // Cell Mol Immunol (2025). DOI: 10.1038/s41423-025-01262-1


 Меню
Меню





 Все темы
Все темы



 0
0